
2025-02-22 00:33:10
磷酸鹽緩沖液取磷酸二氫鈉,與磷酸氫二鈉。磷酸鹽緩沖液()甲液:取磷酸,加水至1000ml,搖勻。乙液:取磷酸氫二鈉,加水使溶解成1000ml。取上述甲液,搖勻,即得。磷酸鹽緩沖液()取磷酸二氫鉀100g,加水800ml,用鹽酸調節pH至。磷酸鹽緩沖液()取,即得。磷酸鹽緩沖液()取磷酸二氫鉀,即得。磷酸鹽緩沖液()取磷酸二氫鉀,用水稀釋至100ml,即得。磷酸鹽緩沖液()取磷酸二氫鈉、磷酸氫二鈉,加水使溶解成400ml,即得。磷酸鹽緩沖液(含胰酶)()取磷酸二氫鉀;另取胰酶10g,加水適量使溶解,將兩液混合后,加水稀釋至1000ml,即得。磷酸鹽緩沖液()取,加,用水稀釋至1000ml,搖勻,即得。磷酸鹽緩沖液()取磷酸二氫鉀,加,用水稀釋至100ml,即得。磷酸鹽緩沖液()取,加新沸過的冷水稀釋至200ml,搖勻,即得。磷酸鹽緩沖液()取磷酸氫二鈉,調節pH值至,即得。磷酸鹽緩沖液()取磷酸二氫鉀,加,用水稀釋至200ml,即得。磷酸鹽緩沖液()取磷酸二氫鉀,加水使溶解成1000ml,取50ml,加,再加水稀釋至200ml,即得。磷酸鹽緩沖液()甲液:取磷酸氫二鈉,加水溶解,并稀釋至500ml。乙液:取磷酸二氫鈉,加水溶解,并稀釋至100ml。取上述甲液,搖勻,即得。磷酸鹽緩沖液(~)取磷酸氫二鉀。緩沖液(Buffer solution)通常是由弱酸及其共軛堿或弱堿及其共軛酸緩沖對所組成的溶液。海南PBS緩沖液常見問題
1MTris-HCl(,,)組份濃度:1MTris-HCl配制量:1L配制方法:1.稱量gTris置于1L燒杯中。2.加入約800ml的去離子水,充分攪拌溶解。3.按下表量加入濃鹽酸調節所需要的pH值。4.將溶液定容至1L。5.高溫高壓**后,室溫保存。注意:應使溶液冷卻至室溫后再調定pH值,因為Tris溶液的pH值隨溫度的變化差異很大,溫度每升高1℃,溶液的pH值大約降低。10&timeTEBuffer(,,)組份濃度:100mMTris-HCl,10mMEDTA配制量:1L配制方法:1.量取下列溶液,置于1L燒杯中。2.向燒杯中加入約800ml的去離子水,均勻混合。3.將溶液定容至1L后,高溫高壓**。4.室溫保存。MTris-HCl()組份濃度:MTris-HCl配制量:1L配制方法:1.稱量gTris置于1L燒杯中。2.加入約800ml的去離子水,充分攪拌溶解。3.用濃鹽酸調節pH值至。4.將溶液定容至1L。5.高溫高壓**后,室溫保存。注意:應使溶液冷卻至室溫后再調定pH值,因為Tris溶液的pH值隨溫度的變化差異很大,溫度每升高1℃,溶液的pH值大約降低。3M醋酸鈉()組份濃度:3M醋酸鈉配制量:100ml配制方法:1.稱量NaAc·3H2O置于100-200ml燒杯中,加入月40ml的去離子水攪拌溶解2.加入冰醋酸調節pH值至3.加去離子水將溶液定容至100ml4高溫高壓**后,室溫保存。江蘇EBSS緩沖液常用知識PBS緩沖液是一種常用的緩沖劑,用于調節pH值和保持溶液的穩定性。
如何計算緩沖溶液的有效PH范圍電離平衡常數的負對數加減1之間。即pK±1之間。例如以醋酸/醋酸鹽為共軛酸堿對的緩沖溶液的有效緩沖范圍是:PKa±1=±1之間。即。緩沖溶液是無機化學及分析化學中的重要概念,緩沖溶液是指具有能夠維持PH相對穩定性能的溶液。pH值在一定的范圍內不因稀釋或外加少量的酸或堿而發生***的變化,緩沖溶液依據共軛酸堿對及其物質的量不同而具有不同的pH值和緩沖容量。擴展資料:緩沖液的pH值與該酸的電離平衡常數Ka及鹽和酸的濃度有關。弱酸的pKa值衡定,但酸和鹽的比例不同時,就會得到不同的pH值。酸和鹽濃度相等時,溶液的pH值與PKa值相同。酸和鹽濃度等比例增減時,溶液的pH值不變。酸和鹽濃度相等時,緩沖液的緩沖效率為比較高,比例相差越大,緩沖效率越低,緩沖液的一般有效緩沖范圍為pH=pKa±1,pOH=pKb±1。在絡合滴定和分光光度法等許多反應里都要求溶液的pH值保持在一個范圍內,以保證指示劑的變色和顯色劑的顯色等,這些條件都是通過加入一定量的緩沖溶液達到的,所以緩沖溶液是分析測試中經常需要的一種試劑。采用電位滴定法測定外加酸或堿對不同配比同一種緩沖溶液的滴定曲線。
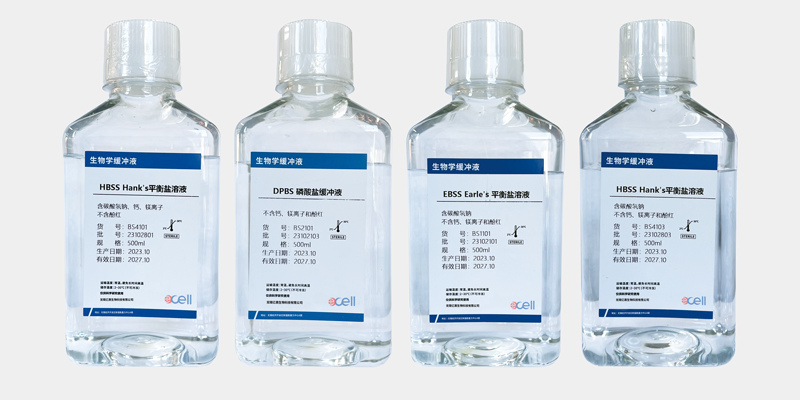
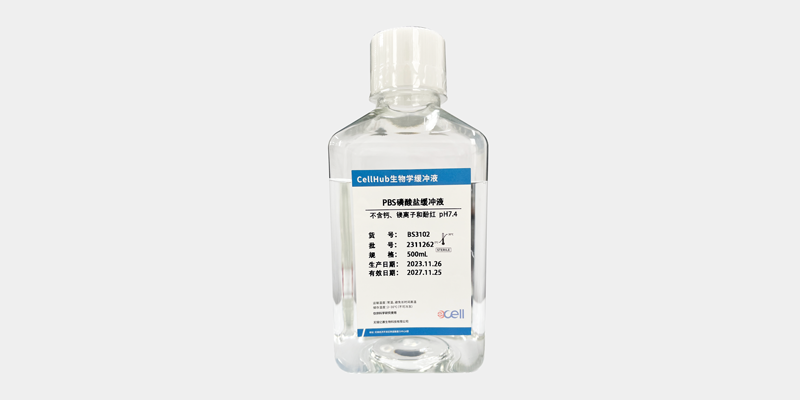
PBS 與 DPBSPBS 和 DPBS 都包括氯化鈉和磷酸鹽緩沖液,是生物學研究中常用的試劑,用于維持 pH 值,同時可大幅度地減少活細胞中的滲透壓休克;然而,與 PBS 相比,DPBS 還包括氯化鉀,配方中可含或不含鈣和鎂以及含或不含葡萄糖和**酸。根據您的具體應用選擇 PBS 或 DPBS。
Dulbecco 的磷酸鹽緩沖液(DPBS)DPBS 與 PBS 的不同之處在于它還包括氯化鉀,并且提供多種配方。它也用于生物應用,水基緩沖液,包括氯化鈉和磷酸鹽緩沖液。
HBSS 與 EBSSHanks 的平衡鹽溶液(HBSS)和 Earle 的平衡鹽溶液(EBSS)都是等滲溶液,用于維持生物應用中的滲透壓和 pH 值。雖然 HBSS 和 EBSS 包括葡萄糖和碳酸氫鈉,用于短期維持生長培養基以外的細胞,但 EBSS 在 5% CO2 下使用,而 HBSS 包含較少的碳酸氫鈉,可以在沒有 CO2 的情況下使用。從各種依應用而定的配方中進行選擇。 什么是緩沖溶液?請簡述其在生物體中的作用。

酶活性實驗中緩沖液的作用在?酶活性實驗中,?緩沖液的主要作用是?維持實驗環境的pH穩定?,為酶提供一個**適的pH環境,從而確保酶的活性得到**佳發揮。緩沖液通過其抗酸抗堿能力,對抗溶液中H+濃度的變化,從而對溶液的酸度起到調節和控制的作用緩沖液的選擇與作用?提供**適pH值?:緩沖液能夠提供酶所需的**適pH值,這對于酶的活性至關重要。不同的酶有不同的**適pH值,通過選擇合適的緩沖液可以確保酶在**佳條件下進行催化反應。?3?維持pH穩定?:緩沖液能夠抵抗外來的酸或堿的影響,保持溶液的pH值相對穩定,從而確保實驗結果的準確性。這對于酶活性實驗尤為重要,因為酶的活性對pH變化非常敏感。?4?提供金屬離子?:在某些情況下,緩沖液還能提供酶所需的金屬離子或其他必要的離子,進一步優化酶的反應條件。 配制緩沖溶液作用有哪些?江蘇EBSS緩沖液常用知識
緩沖液使用中的注意事項。海南PBS緩沖液常見問題
實驗室使用緩沖液時的pH計或酸度計調校方法:1、在對緩沖液使用pH計進行校正時,需要調整儀器的斜率,并將電極上部的橡膠塞撥開,將小孔暴露在外。否則,在校正過程中會產生負壓,導致溶液無法正常進行離子交換,從而使測量數據不準確。2、將電極從燒杯中取出,用濾紙將未干的水分吸干,然后將其放入裝有混合磷酸盆的燒杯中,等待大約15分鐘,然后進行儀器的調整,設定基準點。3、然后將電極放入裝有KHC8H4O4或硼砂溶液的容器中,等待15分鐘后,觀察儀器顯示的pH數值。4、校正完成后,將橡膠塞放回原位。如果暫時不使用pH計,一定要保護好它,將其放入保護套中,以延長其壽命。此外,需要注意的是pH計屬于易碎品,需要輕拿輕放。
手持式緩沖液pH計的校準方法:在溫度為25度的條件下,將測試電極插入pH值為6.86的混合磷酸鹽標準緩沖液中,并緩慢轉動電極。可以稍微調整校正電位器,直到顯示器上的數值與標準緩沖溶液的pH值相同。如果將電極插入其他緩沖溶液中,如pH值為4.01的C8H5KO4或pH為9.18的硼砂標準緩沖溶液中,顯示的數值與緩沖液的pH值允許有一定誤差,但誤差應在參考值范圍內。 海南PBS緩沖液常見問題